Investigadores de España estudiaron la estabilidad de dos clarificantes -proteínas de la clara de huevo (PCH) y caseína- considerados alérgenos potenciales, cuyo límite máximo establecido por la Organización Internacional de la Viña y el Vino (OIV) es de 0,25 mg/l. Los ensayos demostraron que estas proteínas no son estables en el vino y su cuantificación disminuye entre los 30 días y los 6 meses una vez iniciados los estudios en las muestras seleccionadas.

Diversos productos clarificantes son utilizados en las bodegas con la finalidad de eliminar partículas en suspensión, así como elementos inestables presentes en el vino -exceso de taninos, polifenoles, proteínas, metales- y de esta forma, obtener un vino limpio, transparente y estable en el tiempo.
Dos ejemplos de estos productos clarificantes son las proteínas de la clara de huevo (PCH) y la caseína, una importante proteína de la leche. Debido a que ambas moléculas son considerados alérgenos potenciales, sus valores deben declararse en la etiqueta cuando los mismos sean iguales o superiores al límite máximo de 0,25 mg/l establecido por la Organización Internacional de la Viña y el Vino (OIV) y aceptado por la Unión Europea (UE, Reglamento 33/2019). Por este motivo, el objetivo de este trabajo fue investigar la estabilidad de estos alérgenos en una matriz compleja como es el vino.
Se estudió la estabilidad de la PCH y de la caseína en 18 muestras de vino analizadas en la Estación Enológica de Haro (EEH), La Rioja, España, entre 2019 y 2022 mediante el empleo de la técnica «Elisa tipo sandwich». Los ensayos mostraron que estas proteínas no son estables en el vino y su cuantificación disminuye entre los 30 días y los 6 meses una vez iniciados los estudios en las muestras seleccionadas.
Introducción
La práctica enológica conocida como clarificación implica la adición al mosto o al vino de materiales de absorción/adsorción denominados agentes clarificantes, los cuales son empleados para reducir o eliminar la presencia de algunos compuestos no deseados. Por este motivo, el clarificado es un paso fundamental en el proceso de elaboración del vino, ya que ayuda por un lado a reducir el amargor y la astringencia, así como a mejorar la presencia del vino, proporcionando un producto brillante, mucho más atractivo para el consumidor. La clarificación puede modificar el color, la textura o el sabor del vino y, sobre todo, asegurar su estabilidad en el tiempo (Resolución OIV-OENO-SEC- SAN 520-2014).
Algunos de los productos clarificantes utilizados en las prácticas enológicas actuales, son proteínas potencialmente alergénicas que constituyen un motivo de preocupación, ya que pueden inducir una gran variedad de reacciones de hipersensibilidad en personas susceptibles. Por este motivo, el Parlamento Europeo redactó la Directiva 2003/89/CE, modificada por el Reglamento UE 2011/1169, que enumera los alimentos alergénicos que deben declararse en las etiquetas.
En julio de 2012, se declaró obligatorio indicar en las etiquetas el uso de productos derivados de la leche o del huevo siempre que se utilicen como clarificantes y se detecten en el vino (Reglamento UE 33/2019) en niveles iguales o superiores a 0,25 mg/l. Para detectar trazas de estos agentes clarificantes en el vino, se han desarrollado ensayos inmunoenzimáticos Elisa muy sensibles para la detección de trazas.
Sin embargo, tras la revisión de una amplia bibliografía, no se encontraron estudios que evalúen la estabilidad de estos alérgenos una vez detectados en el vino. Por este motivo, el laboratorio de microbiología de la Estación Enológica de Haro estudió la estabilidad de estos alérgenos a lo largo del tiempo tanto en vinos dopados experimentalmente como en muestras naturales.
Materiales y métodos
Conservación de las muestras: Los resultados mostrados en este trabajo, corresponden a muestras que se conservaron a temperatura ambiente entre (20-25 ºC).
Selección de muestras para el ensayo y cuantificación de proteínas: Las muestras recibidas en el laboratorio en el período comprendido entre 2019 y 2022, que una vez analizadas dieron valores positivos (> LC del método), fueron seleccionadas para los estudios. Se hizo un seguimiento de los alérgenos en cada muestra de vino realizando análisis periódicos sobre las mismas hasta que el valor de proteína (mg/l), fue inferior al límite de cuantificación de ambos métodos. Cada muestra se ensayó en duplicado mediante la técnica de Elisa tipo sándwich (ensayo inmunoenzimático), acreditada en la matriz vino por ENAC (Acreditación Nº 183/LE407).
Se utilizaron dos kits comerciales de diagnóstico, Ridas-Creen Fast Egg Protein (Ref; R6402) de R-Biopharm y Casein (Ref; 14113) de BioSystems, para la cuantificación de la proteína de la clara de huevo (PCH) y de la caseína (CAS), respectivamente. La extracción de ambos alérgenos se realizó siguiendo las instrucciones de ambos fabricantes.
Brevemente, para la PCH se mezcló 1 ml de la muestra de vino previamente homogeneizada con 19 ml de tampón de extracción, mientras que para la extracción de CAS se añadieron 0,5 ml de muestra a 9,5 ml de tampón de extracción. Posteriormente, las muestras se incubaron a 60ºC durante 10 y 15 minutos respectivamente. Antes de su aplicación por duplicado en la placa de ELISA, las muestras se atemperaron entre 20 y 25 ºC.
Las soluciones Biosystem Egg White (Ref;14158) y Casein (Ref; 14151) se utilizaron como “spikes” para preparar los controles positivos con el fin de evaluar la recuperación a diferentes niveles de concentración. Los límites de cuantificación (LC) de los métodos acreditados utilizados para la determinación de PCH y Caseína son de 0,13 mg/l y 0,20 mg/l respectivamente. Ambos LC son inferiores al límite definido por la OIV (0,25 mg/l) para su consecuente declaración obligatoria en etiqueta según el Reglamento Europeo, sobre la presencia de alérgenos en el vino.
Resultados
En la EEH se analiza anualmente un gran número de muestras y cabe destacar que menos del 5% son positivas (muestras con resultados mayores que LC del método utilizado) para cualquiera de los dos alérgenos analizados (Tabla 1).
Durante el periodo de estudio, de 1643 muestras analizadas para PCH y 1822 para caseína, sólo el 1,2% y el 0,7 % respectivamente superaron el límite establecido (0,25 mg/l). Dieciocho de estas muestras con diferentes concentraciones de alérgenos fueron seleccionadas para el estudio.
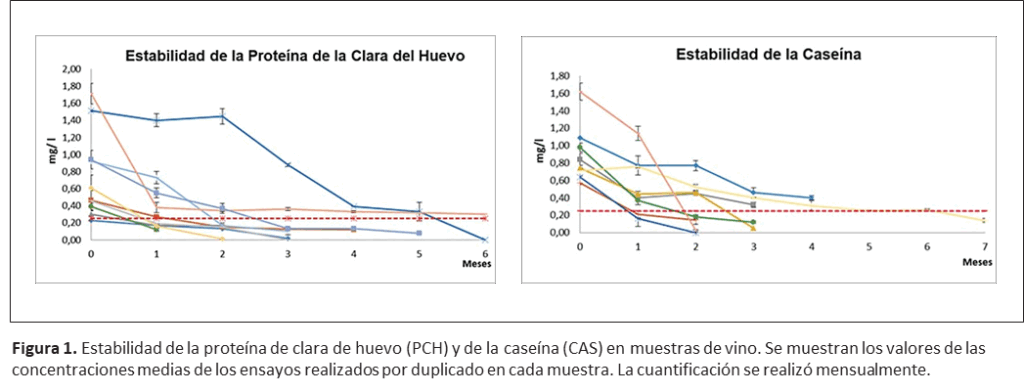
Los ensayos mostraron que los analitos estudiados evidencian una inestabilidad en el vino, las concentraciones de ambas proteínas disminuyeron con el tiempo durante la duración del estudio (Figura 1).
Se demostró que esta inestabilidad era independiente de la concentración de alérgenos en el vino de partida, es decir, que muestras con concentraciones iniciales elevadas podían disminuir rápidamente mientras que otras con concentraciones iniciales más bajas, podían persistir y cuantificarse en el vino durante un periodo de tiempo más prolongado.
Por otra parte, se observó que esta inestabilidad también era independiente de la temperatura de almacenamiento de la muestra, aunque mostraban ser más estable cuando las mismas fueron conservadas a -20ºC (datos no mostrados).
Discusión
La PCH y la caseína son productos comerciales utilizados por muchos enólogos para mejorar la calidad del vino. El potencial alergénico de estos dos productos es ampliamente conocido.
Una pregunta importante a la que teníamos que dar respuesta fue conocer cuánto tiempo podían permanecer estas proteínas en el vino después de su tratamiento en las bodegas. Los estudios revelaron que tanto las proteínas de la clara de huevo como la caseína eran inestables durante el almacenamiento del vino.
Esto puede deberse a un cambio conformacional (agregación, desenrollamiento, plegamiento) o a la degradación de estas moléculas debido a la complejidad de la matriz, que puede afectar su detección por los detectores del kit, es decir, los anticuerpos empleados. La modificación de la estructura de estas proteínas clarificantes puede afectar el reconocimiento antígeno/anticuerpo. Por otra parte, el cambio conformacional no implica necesariamente una pérdida de alergenicidad de las proteínas estudiadas, dependerá de qué tipo de epítopo (lineal o conformacional) intervenga en el mecanismo desencadenante de la respuesta inmune.
Para entender la pérdida de estabilidad de estas proteínas en el vino, debemos comprender los factores que actúan sobre la conformación nativa de estas proteínas que pueden desestabilizarlas y, en consecuencia, llevar al cambio reversible o no de su estructura.
Hay algunos factores que deben tenerse en cuenta al estar estos relacionados con la estabilidad de las proteínas, dos de estos factores son el pH y la temperatura del medio en el que se encuentran las proteínas. Los vinos tratados durante el proceso de clarificación, tienen un pH ácido. Hegg y col., 1979 encontraron que la ovoalbúmina, principal proteína de la PCH, tiene una estabilidad máxima a valores de pH entre 6-10, valores muy distantes a los pH del vino. Sin embargo, en un estudio realizado por Koseki y colaboradores, en 1988, los autores indicaron que la conformación globular de la ovoalbúmina a pH ácido es similar a la de pH neutro, y encontraron que las moléculas se volvían más flexibles a medida que el pH disminuía.
En relación con la caseína (aproximadamente el 80 % de la proteína total de la leche), forma una estructura coloidal, un biocoloide, conocido como micela de caseína. Estudios recientes han demostrado que las micropartículas obtenidas a partir de micelas de caseína permanecen estables en el intervalo de pH ácido y neutro, sin embargo, la concentración de calcio y citrato, dos elementos químicos presentes en los vinos, influye significativa- mente en la estabilidad de las caseínas.
Todo lo explicado anteriormente sugiere que el pH del vino per se, no parece ser el factor crítico en la pérdida de estabilidad de estos alérgenos utilizados como agen- tes clarificantes.
La temperatura es otro factor importante a tener en cuenta para la estabilidad de las proteínas, ya que generalmente su estructura sufre cambios irreversibles cuando se someten a altas temperaturas, llegando a su desnaturalización. En relación con esta, hay que decir que el almacenamiento de los vinos raramente supera los 20ºC, y en muchos casos se almacenan a temperaturas más bajas, que oscilan entre 14 y 18ºC, lo cual puede favorecer la estabilidad de los alérgenos en el tiempo.
Estudios preliminares obtenidos en nuestro laboratorio donde se comparó la estabilidad de estas proteínas a diferentes temperaturas (datos no publicados), evidenciaron que estos dos alérgenos fueron más estables cuando los vinos fueron almacenaron a -20ºC (temperatura no utilizada en la práctica comercial).
Otro factor no menos importante a tener en cuenta en los estudios de estabilidad de la PCH y la caseína, son los niveles de alcohol (grado alcohólico) del vino donde se encuentran estos agentes clarificantes. De acuerdo a la definición de la OIV, los vinos presentan valores de alcohol adquirido superiores a 8,5% vol. Paulinelli y col., (1997) describen que la ovoalbúmina, la proteína mayoritaria de la PCH, tiene dos formas, una forma nativa y la forma «ovoalbúmina S», la cual presenta una estructura secundaria termoestable. Miyakami, en 1988, estudió el efecto de los alcoholes sobre la estabilidad de estas variantes, el autor demostró que la forma «S» de la ovoalbúmina es más estable en presencia de alcohol que la forma nativa. Este estudio confirma que la inestabilidad creada por los alcoholes depende de sus grupos alquilo y sus ramificaciones, que interfieren creando inestabilidad en el núcleo hidrofóbico de la molécula. Por otra parte, otros estudios realizados con estructuras micelares de caseína por Kruzely col., (2004), demostraron que el alcohol inducía cambios conformacionales en la estructura de esta proteína.
Teniendo en cuenta lo explicado anteriormente, se entiende que tanto los factores mencionados con anterioridad, así como otros asociados a los componentes propios de esta matriz, deben influir en mayor o menor medida en la pérdida de la estabilidad observada en estas moléculas. Podría pensarse que la unión de estas proteínas clarificantes a compuestos estructuralmente complejos y variados como los polifenoles para formar agregados moleculares, afecten la estabilidad de las mismas y consecuentemente también su detección y cuantificación.
Conclusiones
El estudio demostró la inestabilidad en el tiempo de las proteínas empleadas como clarificantes del vino (PCH y caseína) y que, por consiguiente, la fecha de análisis de estos alérgenos influye en su detección. La estabilidad de estas proteínas duró aproximadamente entre uno a seis meses, dependiendo de cada muestra de vino y fue independiente de su concentración inicial o de partida.
El porcentaje de vinos con valores superiores al límite legal establecido por la Organización Internacional de la Viña y el Vino para su declaración obligatoria (0,25mg/l) fue bajo (aproximadamente el 1%).
Otros estudios serán necesarios para poder evaluar los cambios estructurales en ambos alérgenos, así como su correlación con la pérdida o no de alergenicidad de estas proteínas. El presente trabajo no puede dar respuesta a estas cuestiones.
Fuente: Revista Enólogos – Autores: Carolina Gómez Sordo, Elena Meléndez Álvarez, Óscar Hernández Betancourt (Estación Enológica de Haro. Laboratorio de Microbiología. Bretón de los Herreros (La Rioja) España. Autor de contacto cgomezs@larioja.org